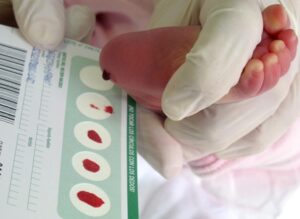
Este tipo de biopsia evita al paciente trastornos innecesarios y representa un ahorro de tiempo ya que los resultados de los análisis están disponibles en pocos días, mientras que la biopsia tumoral puede llegar a tardar más de un mes.
El procedimiento es sencillo, se podrá repetir las veces que se considere necesario realizar, para controlar la evolución de una patología que no es estática sino cambiante.
A diferencia de las biopsias tumorales, que son invasivas y potencialmente dolorosas, para la biopsia líquida sólo se requiere de una extracción de 20 ml de sangre.
Conocer mejor la biología y la genética del tumor facilita las decisiones que deban tomarse respecto al tratamiento, pudiéndose adaptar a las características específicas de cada cáncer.
Cuando hay un ¨tumor¨, se libera material genético, proteínas y células cancerígenas en el torrente sanguíneo. Los tumores en situación ¨metastásica¨ liberan células, y por tanto material genético en el torrente sanguíneo.
Con una extracción de sangre se puede detectar este ADN circulante, células tumorales y otros compuestos propios del tumor.
Las técnicas para la detección del ADN circulante y de células tumorales deben ser ultrasensibles, estos compuestos y células se encuentran en una proporción extremadamente baja en la sangre.

La detección del ADN de las células tumorales nos permite determinar la evolución de la enfermedad y seleccionar los tratamientos para tratar el tumor específicamente.
De esta manera se identifican mutaciones, copias génicas, genes implicados en el desarrollo de tumores sólidos, cánceres hereditarios, e inestabilidad de microsatélites (metástasis), que son secuencias cortas de ADN que no codifican para ningún gen pero constituyen marcadores genéticos en algunos cánceres.
¨Disponemos de datos que nos indican que en los estadios precoces la biopsia líquida puede lograr el diagnóstico del cáncer de pulmón antes de que sea visible mediante imagen”.
Así lo ha manifestado el doctor Ignacio Wistuba, del Departamento de Patalogía Molecular Traslacional del Servicio de Anatomía Patológica del MD Anderson Cancer Center de Houston (Texas), en el marco del Early Forum Virtual en cáncer de pulmón, organizado por el Grupo Español de Cáncer de Pulmón (GECP) y Roche Farma España, y centrado en analizar los retos en la detección y tratamiento de esta enfermedad en fases iniciales.
“Gracias a la cada vez mayor sensibilidad de la biopsia líquida se podría utilizar para identificar precozmente en un paciente posibles recaídas.
¨Es imprescindible”, explica el doctor Wistuba, “definir el perfil molecular en las fases iniciales de esta enfermedad para poder ofrecer opciones terapéuticas, como son las terapias dirigidas o la inmunoterapia, a pacientes con alteraciones moleculares, antes (neoadyuvancia) o después (adyuvancia) de la cirugía, aumentando su supervivencia a más de cinco años, así como, las tasas de curación”.
El desarrollo de nuevas tecnologías y el refinamiento de las técnicas moleculares han ofrecido la posibilidad de estudiar nuevos biomarcadores en el campo de la oncología, entre los que se encuentran los ácidos nucleicos circulantes.
Aquellos con mayor evidencia clínica son: el ADN libre circulante (cell-free DNA, cfDNA), el ADN tumoral circulante (circulating tumor DNA, ctDNA) y el ARN libre circulante (cell-free RNA, cfRNA); son ácidos nucleicos derivados tanto del tumor como de células tumorales circulantes (CTCs) y de exosomas.
Su análisis ha permitido clasificar los tumores de manera más precisa y menos invasiva, mediante la descripción de perfiles genómicos. Se establece su asociación directa a un adecuado diagnóstico y pronóstico, y la selección de tratamientos dirigidos, en consecuencia la predicción de la respuesta terapéutica.
Las células tumorales circulantes (CTCs) se originan a partir del tumor primario, que al separarse del tejido tumoral ingresan al sistema vascular, desde donde pueden migrar a otros tejidos dando origen a las metástasis.
Su liberación y eliminación es constante a lo largo del curso neoplásico.
En sujetos sanos o con enfermedades no malignas, los niveles de CTCs son inexistentes, mientras que niveles detectables de estas células se han encontrado en pacientes con carcinomas metastásicos de pulmón, próstata, mama, colón, entre otros.
El estudio desarrollado por el Dr. Aleix Prat y el Dr. Javier García-Corbacho del Hospital Clínic de Barcelona ha analizado el perfil genético de 321 pacientes oncológicos con tumores sólidos.
Se realizó mediante biopsia líquida en sangre con Guardant360 , una prueba capaz de analizar 74 genes mediante técnicas de secuenciación masiva y se detectaron alteraciones genómicas en el 90% de los casos.
El estudio, que empezó en septiembre del año pasado, estableció una ¨secuenciación genómica¨ de los tumores a lo largo de 18 meses.
El objetivo fue seleccionar la terapia más adecuada según la evolución de la enfermedad en cada paciente.
Se analizaron muestras de tumores pulmonares, pancreáticos, colorrectales, colangiocarcinoma, de mama, de tiroides y carcinoma de glándulas salivales.
La sensibilidad de la prueba es muy elevada ya que se detectaron alteraciones genómicas en prácticamente el 90% de los casos, lo cual abre la puerta a una potencial terapia dirigida contra cada tipo de cáncer.
Esta prueba debe ser ¨interpretada¨ para seleccionar el tratamiento correcto, por ello, se han empezado a crear grupos de especialistas (tumor molecular board) que revisan cada caso y emiten una recomendación conjunta.
¨Permite la determinación a tiempo real de las características genéticas del tumor, sin duda, va a aumentar la supervivencia de nuestros pacientes”. Comenta el Dr. Javier García-Corbacho
Por otra parte, el Instituto de Oncología de Vall d’Hebron de Barcelona será el primer centro científico en el mundo en utilizar esta técnica, que inicialmente servirá para detectar biomarcadores RAS (KRAS y NAS) en pacientes con cáncer¨ colorrectal metastásico¨.
La mitad de los casos podrán recibir tratamientos específicos para esas mutaciones.
La Oncología Médica se dirige hacia una prescripción personalizada de la medicación por lo que sin duda el análisis del ADN circulante formará parte de las consultas en el futuro.
Conocer cómo es el tumor y qué alteraciones presenta a través de la biopsia líquida, es clave para poder seleccionar la mejor terapia en cada caso e incluso estudiar la evolución del tratamiento y de la propia enfermedad, identificando mecanismos de resistencia a terapias.
Será un avance importante para lograr a una medicina de precisión.